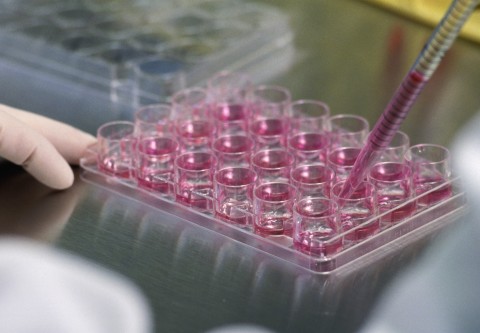
 Cellule staminali embrionali: ovvero, grande potenzialità terapeutica e molti limiti etici. La FDA americana però, per la seconda volta dall’inizio dell’anno ha autorizzato la sperimentazione clinica (ovvero su delle persone malate) di nuove terapie che utilizzano queste cellule staminali immature, capaci di evolversi in tessuti sani.
Cellule staminali embrionali: ovvero, grande potenzialità terapeutica e molti limiti etici. La FDA americana però, per la seconda volta dall’inizio dell’anno ha autorizzato la sperimentazione clinica (ovvero su delle persone malate) di nuove terapie che utilizzano queste cellule staminali immature, capaci di evolversi in tessuti sani.
L’autorizzazione in questione è stata data alla Advanced Cell Tecnology che intende testare una sua cura a base di cellule staminali embrionali su 12 piccoli pazienti affetti da distrofia maculare di Stargardt. Questa patologia colpisce infatti in giovane età, tra i 10 ed i 20 anni (la casistica più alta riguarda i bambini tra i 7 ed i 12 anni) e attualmente non è curabile.
L’alterazione di un unico gene provoca la degenerazione dell’epitelio pigmentato retinico (Rpe-un tessuto dell’occhio) causando una progressiva perdita della vista fino alla totale cecità. La Advanced Cell Tecnology è riuscita a riprodurre i tessuti sani del Rpe utilizzando cellule staminali embrionali: ora potrà applicarli agli occhi dei bambini malati ed aspettare i risultati, che si prospettano piuttosto incoraggianti. La malattia di Stargardt colpisce una persona ogni 20/30.000.
Dicevamo che è il secondo caso dall’inizio dell’anno di autorizzazione da parte dell’FDA a queste pratiche molto discusse. L’altra è stata ottenuta dall’azienda biotecnologica Geron Corporation che a Ottobre ha iniziato la sperimentazione: rigenerare il midollo spinale lesionato di un paziente paralizzato. In questo caso le cellule staminali prelevate da embrione umano sono state fatte sviluppare per ricostituire la protezione delle fibre nervose: una volta iniettate, trapiantate sul paziente dovrebbero “specializzarsi”, cioè completare il loro sviluppo e permettere nuovamente la formazione di mielina (ovvero di quella membrana che protegge i neuroni e permette loro di trasmettere segnali e messaggi atti al movimento).
Sui topi di laboratorio della Geron il test ha funzionato. Ora prima di parlare di cura, lo studio clinico su un paziente umano, dovrà dimostrare la sicurezza della terapia, garantire cioè che non provochi effetti collaterali.
In ambedue i casi autorizzati dall’amministrazione americana occorrerà aspettare i risultati certi.
[Fonte: Reuters]
